卡瑞珠单抗联合阿帕替尼治疗宫颈癌最新数据
宫颈癌是女性第4大常见恶性肿瘤,是最常见的妇科恶性肿瘤。根据最新癌症相关统计数据,我国每年宫颈癌新发病例约10万例,约3万人死于宫颈癌。晚期及复发宫颈癌的治疗手段有限,5年生存率不到20%。
除了传统的手术、放疗和化疗外,抗血管生成靶向治疗和肿瘤免疫治疗取得了显著的疗效,但一线治疗后进展的晚期宫颈癌患者治疗选择有限。
虽然美国食品药物监督管理局(FDA)批准PD-1抑制剂派姆单抗用于晚期及复发宫颈癌的治疗,但单药治疗有效率却不尽如人意,临床亟需新的治疗模式改善这部分患者的治疗现状。
2020年3月28日,美国妇科肿瘤学会(SGO)官网公布了一项多中心、开放标签、单臂II期研究结果,评估了卡瑞利珠单抗联合阿帕替尼作为晚期宫颈癌二线或后线治疗的疗效及安全性。
美国妇科肿瘤学会是全球首屈一指的专业致力于妇科肿瘤的研究、治疗与教育的非营利性医学组织。拥有50余年历史的美国妇科肿瘤学会,因其精准聚焦妇科肿瘤,内容全面且深入,兼顾基础及临床学术前沿,一直是国际上最负盛名的妇科肿瘤学术年会。

商品名:艾瑞卡
通用名:卡瑞利珠单抗(camrelizumab)
厂家:恒瑞
美国首次获批:尚未获批
中国首次获批:2019年5月5日
获批适应症:复发或难治性经典型霍奇金淋巴瘤、肝癌
规格:200mg/瓶
推荐剂量:每次200mg,每2周一次
价格:19800/瓶
赠药方案:买2赠2,再买4赠至一年(不超过18支)。也就是说符合赠药条件的患者在自费2个周期后可以获得接下来2个周期的慈善赠药;再次购买4个周期后,在符合赠药条件下,后续可获得赠至一年疗程(从第一支使用计算起的一整年)的援助。
试验设计
该研究采用Simon二阶段的设计,第一阶段入组16例患者,如果超过3例缓解,研究将扩展至第二阶段。
Simon二阶段
临床试验单臂设计分为单阶段设计和多阶段设计(二,三阶段)。Simon二阶段(Simon2)设计目前应用最为广泛的二阶段设计方法。
Simon2的基本原理是:第一阶段先入组n1例患者,如果r1例或者更少的患者有效,则认为试验药物无效,需要终止研究;如果超过r1例患者有效,则继续入组n2例患者进入第二阶段,如果在总的N=n1+n2例患者中总的有效病例数(包括第一阶段的有效病例数)小于或等于第二阶段临界值r,则认为试验药物无效。若有效病例数大于临界值r,该药物可进行后续临床试验研究继续评估疗效。
入组患者接受卡瑞利珠单抗(每2周一次200mg)联合阿帕替尼(每日一次250mg)治疗。
入组人群为组织学证实为转移性、复发性或持续性宫颈癌患者;年龄18-70岁;ECOG评分0-1;至少接受了一线系统治疗后疾病进展;至少有一处可评估病灶。
研究的主要终点为研究者评估的客观有效率(ORR),次要终点包括无进展生存(PFS)、总生存(OS)、缓解持续时间(DOR)、疾病控制率(DCR)和安全性。探索性研究的终点为PD-L1表达与疾病缓解、PFS的相关性。
临床数据
第一阶段入组16例患者,共观察到8例缓解。研究继续扩展到第二阶段,最终共入组45例患者。
截至2020年1月22日数据,总共42例患者进行了至少一次的肿瘤评估:客观缓解率(ORR)为59.5%(25/42);完全缓解(CR)率为4.8%(2/42);疾病稳定(SD)率为28.6%(12/42);疾病控制率(DCR)为88.1%;73.3%的患者(33/42)肿瘤病灶直径较基线缩小;中位缓解持续时间(DOR)为1.9个月,尚未达到;中位无进展生存期(PFS)为7.6个月;中位生存期(OS)尚未达到。
 图注:卡瑞利珠单抗联合阿帕替尼治疗宫颈癌患者的PFS
图注:卡瑞利珠单抗联合阿帕替尼治疗宫颈癌患者的PFS
探索性研究发现:PD-L1阳性患者 VS PD-L1阴性患者的中位PFS为9.6个月 VS 5.3个月;ORR为69% VS 50%。
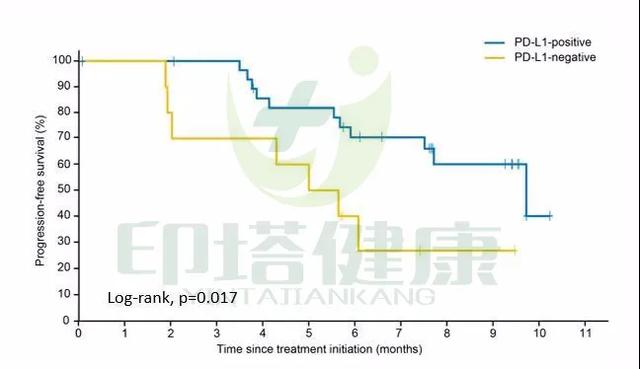 图注:卡瑞利珠单抗联合阿帕替尼治疗PD-L1阳性患者 VS PD-L1阴性宫颈癌患者的中位PFS
图注:卡瑞利珠单抗联合阿帕替尼治疗PD-L1阳性患者 VS PD-L1阴性宫颈癌患者的中位PFS
不良反应
最常见的治疗相关3/4级不良反应(>5%)有:高血压(24.4%)、贫血 (20%)、乏力(15.6%)、中性粒细胞减少(6.7%)、血小板下降(6.7%)。
最常见的免疫治疗相关1/2级不良反应有:甲状腺功能减退(22.2%)。未发生治疗相关的死亡事件。
小结
卡瑞利珠单抗联合阿帕替尼在晚期宫颈癌患者中显示出良好的抗肿瘤活性和可耐受的毒性。
【重要提示】本公号【全球好药资讯】所有文章信息仅供参考,具体治疗谨遵医嘱!



