国产第三代新型EGFR-TKI:伏美替尼正式上市
2021年3月3日,国家药品监督管理局(NMPA)批准了甲磺酸伏美替尼上市,用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。
伏美替尼是一种不可逆、选择性的第三代EGFR抑制剂,对EGFR T790M+敏感突变具有显著的抑制活性。
截止现在,国内已有3款第三代EGFR-TKI上市:奥希替尼、阿美替尼、伏美替尼。
商品名:艾弗沙
通用名:甲磺酸伏美替尼
靶点:EGFR
获批适应症:非小细胞肺癌(NSCLC)
临床数据
1、客观缓解率为74.1%,疾病控制率达93.6%!
2019年11月,伏美替尼治疗EGFR T790M突变阳性局部晚期或转移性NSCLC的适应证申请递交国家药品监督管理局,并获得优先审评和审批资格。该适应证申请是基于伏美替尼的一项开放标签、多中心、单臂的Ⅱb期关键注册临床研究(NCT03452592)。
该IIb期研究结果已于2020年美国临床肿瘤学会(ASCO)年会上发布。该研究纳入220例携带EGFR T790M突变的、既往接受一/二代EGFR-TKI进展或原发性EGFR T790M突变的、局部晚期或转移性NSCLC患者,给予80mg/d伏美替尼治疗。在入组患者中有48%基线CNS转移的患者,38% L858R突变和4% PS评分2分的患者。
研究的主要终点为客观缓解率(ORR),次要终点包括疾病控制率(DCR)、缓解持续时间(DOR) 、无进展生存(PFS)、安全性等。
Ⅱb期研究结果显示:伏美替尼治疗EGFR T790M突变阳性晚期NSCLC的ORR为74.1%;DCR为93.6%;PFS为9.6个月;临床获益率(CBR)为79.5%;中位PFS为9.6个月,中位缓解持续时间(mDOR)为8.3个月。
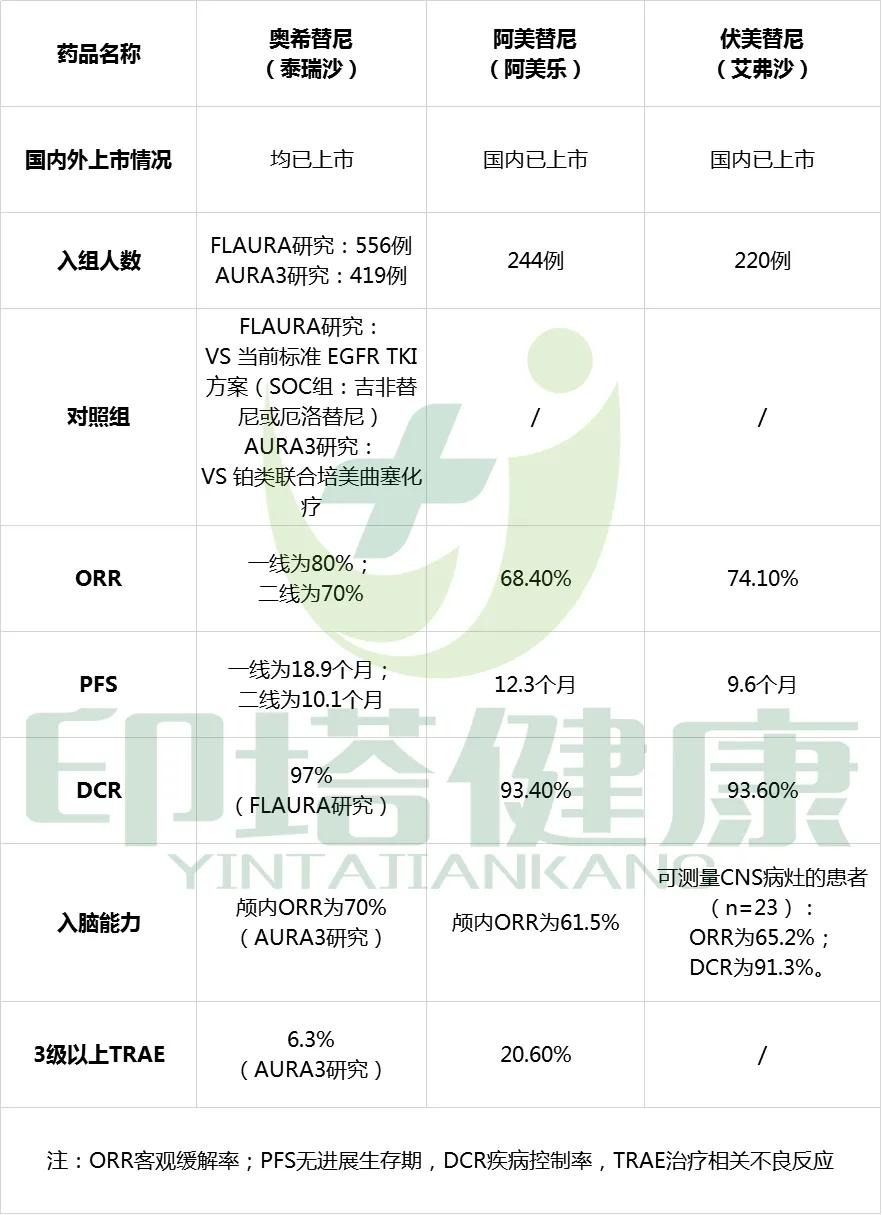
图注:国内已上市的第三代EGFR-TKI(奥希替尼、阿美替尼、伏美替尼)数据列表
2、治疗脑转移NSCLC研究数据亮相2020WCLC
2021年1月13日,伏美替尼治疗中枢神经系统(CNS)转移非小细胞肺癌的人群亚组分析结果以摘要形式正式在第21届世界肺癌大会(WCLC 2020)官网公布。
该研究结果来自于伏美替尼治疗EGFR T790M突变阳性局部晚期或转移性NSCLC的I-II期剂量扩展研究(NCT03127449)。
伏美替尼治疗EGFR T790M突变阳性局部晚期或转移性NSCLC的I-II期剂量扩展研究纳入了116例EGFR T790M突变阳性、ECOG 评分为0~2分的NSCLC患者,包括了无症状和稳定的CNS转移患者。给予不同剂量的伏美替尼(40mg/d、80mg/d、160mg/d、240mg/d)治疗,直至疾病进展或出现不可耐受的毒性。
基线时有≥1个可测量和/或不可测量CNS病灶的患者为45例(38.8%),其中有≥1个可测量CNS病灶的患者为23例(19.8%)。
截至2020年1月29日,临床数据显示:在23例可测量CNS病灶的患者中,总的CNS 客观缓解率(ORR)为65.2%;CNS疾病控制率(DCR)为91.3%;
40mg/d剂量组 VS 80mg/d剂量组 VS 160mg/d剂量组 VS 240mg/d剂量组的ORR为0% VS 60% VS 84.6% VS 25%;DCR为0% VS 80% VS 100% VS 100%。
在45例可测量和/或不可测量CNS病灶的患者中,总的无进展生存期(PFS)为未达到(NR);40mg/d剂量组 VS 80mg/d剂量组 VS 160mg/d剂量组 VS 240mg/d剂量组的PFS 为2.8个月 VS 9.7个月 VS 19.3个月 VS NR。
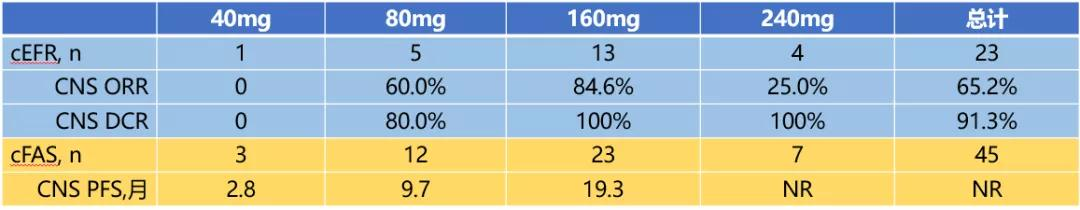
图注:不同剂量组CNS转移患者疗效结果
这一亚组分析结果表明,伏美替尼用于CNS转移NSCLC患者的疗效具有临床意义。160mg组具有更高的CNS ORR和更长的CNS PFS。这一数据为伏美替尼用于CNS转移患者的治疗提供了有力支持。
结论
伏美替尼本次获批上市将为非小细胞性肺癌(NSCLC)成人患者提供了新的治疗选择。
【重要提示】本公号【全球好药资讯】所有文章信息仅供参考,具体治疗谨遵医嘱!



